Нат Мед | Мулти-омички приступ мапирању интегрисаног туморског, имуног и микробног пејзажа колоректалног карцинома открива интеракцију микробиома са имуним системом
Иако су биомаркери за примарни рак дебелог црева опширно проучавани последњих година, тренутне клиничке смернице се ослањају само на стадијум тумора, лимфних чворова и метастаза и детекцију дефеката поправке неусклађености ДНК (MMR) или микросателитске нестабилности (MSI) (поред стандардног патолошког тестирања) како би се одредиле препоруке за лечење. Истраживачи су приметили недостатак повезаности између имуних одговора заснованих на експресији гена, микробних профила и строме тумора у кохорти колоректалног карцинома Атласа генома рака (TCGA) и преживљавања пацијената.
Како су истраживања напредовала, објављено је да квантитативне карактеристике примарног колоректалног карцинома, укључујући ћелијску, имунолошку, стромалну или микробну природу рака, значајно корелирају са клиничким исходима, али још увек постоји ограничено разумевање како њихове интеракције утичу на исходе пацијената.
Да би анализирали везу између фенотипске сложености и исхода, тим истраживача из Института за медицинска истраживања Сидра у Катару недавно је развио и валидирао интегрисани скор (mICRoScore) који идентификује групу пацијената са добрим стопама преживљавања комбиновањем карактеристика микробиома и константи имунолошког одбацивања (ICR). Тим је извршио свеобухватну геномску анализу свеже замрзнутих узорака од 348 пацијената са примарним колоректалним карциномом, укључујући секвенцирање РНК тумора и упареног здравог колоректалног ткива, секвенцирање целог ексома, секвенцирање дубоког Т-ћелијског рецептора и 16S бактеријске рРНК гена, допуњено секвенцирањем целог туморског генома како би се даље окарактерисао микробиом. Студија је објављена у часопису Nature Medicine под називом „Интегрисани туморски, имуни и микробиомски атлас рака дебелог црева“.

Чланак објављен у часопису Nature Medicine
Преглед AC-ICAM-а
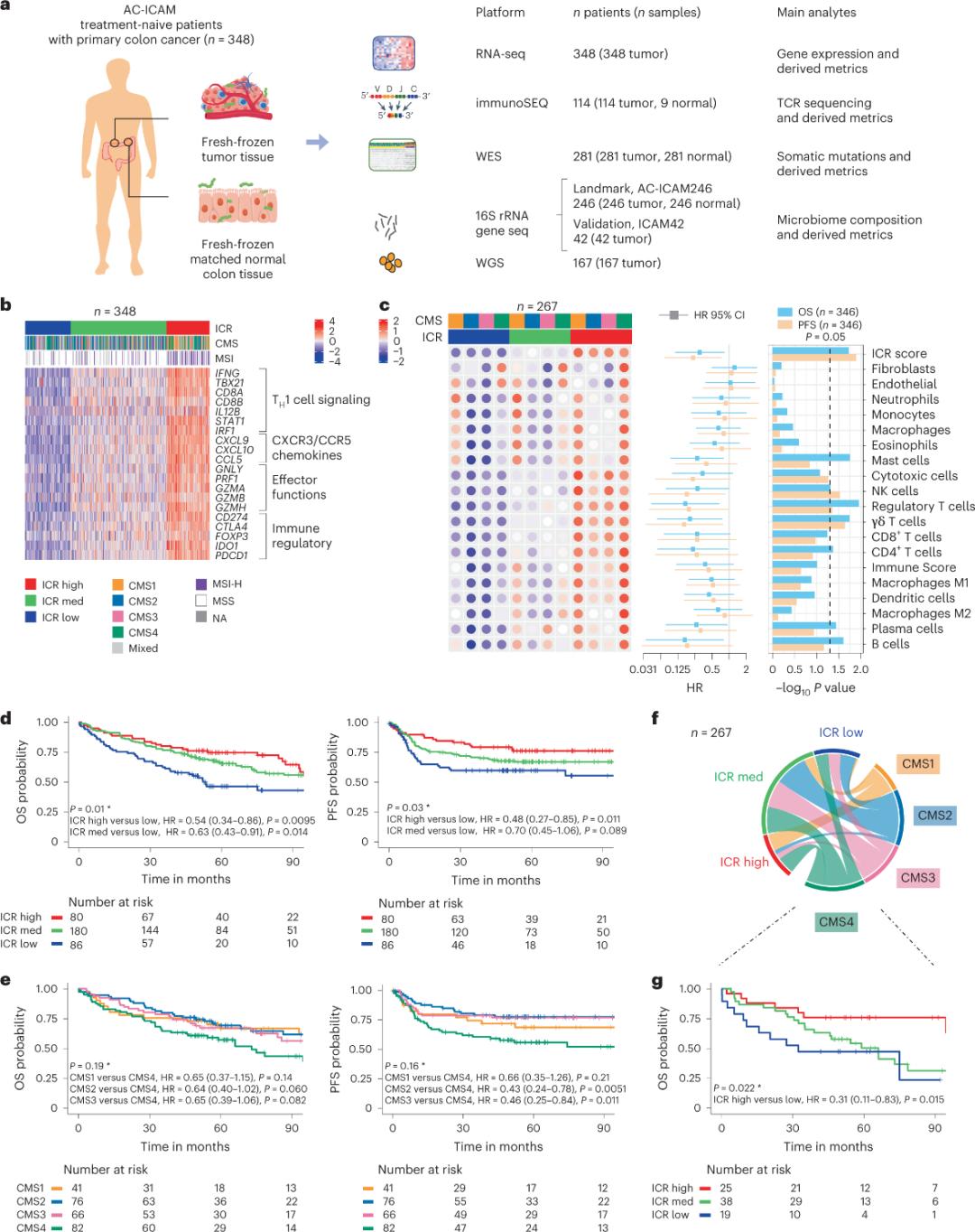
Истраживачи су користили ортогоналну геномску платформу за анализу свеже замрзнутих узорака тумора и упареног суседног здравог ткива дебелог црева (парови тумор-нормално ткиво) од пацијената са хистолошком дијагнозом рака дебелог црева без системске терапије. На основу секвенцирања целог ексома (WES), контроле квалитета података RNA-seq и скрининга критеријума за укључивање, геномски подаци од 348 пацијената су сачувани и коришћени за даљу анализу са средњим временом праћења од 4,6 година. Истраживачки тим је назвао овај ресурс Sidra-LUMC AC-ICAM: Мапа и водич за интеракције имунитета, рака и микробиома (Слика 1).
Молекуларна класификација коришћењем ICR-а
Истраживачки тим је оптимизовао модуларни скуп имунолошких генетских маркера за континуирани имунолошки надзор рака, назван имунолошка константа одбацивања (ICR), тако што га је кондензовао у панел од 20 гена који покрива различите врсте рака, укључујући меланом, рак бешике и рак дојке. ICR је такође повезан са имунотерапијским одговором код различитих врста рака, укључујући рак дојке.
Прво, истраживачи су валидирали ICR потпис AC-ICAM кохорте, користећи приступ кокласификације заснован на ICR генима како би класификовали кохорту у три кластера/имунолошких подтипа: висок ICR (врући тумори), средњи ICR и низак ICR (хладни тумори) (Слика 1б). Истраживачи су окарактерисали имунолошку склоност повезану са консензусним молекуларним подтиповима (CMS), класификацијом рака дебелог црева заснованом на транскриптомима. CMS категорије су укључивале CMS1/имунолошки, CMS2/канонски, CMS3/метаболички и CMS4/мезенхимални. Анализа је показала да су ICR резултати негативно корелирани са одређеним путевима ћелија рака у свим CMS подтиповима, а позитивне корелације са имуносупресивним и путевима повезаним са стромалом примећене су само код CMS4 тумора.
У свим ЦМС, обиље подскупова природних ћелија убица (НК) и Т ћелија било је највеће код подтипова ИЦР са високим имунитетом, са већом варијабилношћу код осталих подскупова леукоцита (Слика 1ц). Имуни подтипови ИЦР имали су различито преживљавање без прогресије болести (ОС) и преживљавање без прогресије болести (ПФС), са прогресивним повећањем ИЦР од ниског до високог (Слика 1д), што потврђује прогностичку улогу ИЦР код колоректалног карцинома.
Слика 1. Дизајн AC-ICAM студије, имунолошки повезани генски потпис, имунолошки и молекуларни подтипови и преживљавање.
ИЦР хвата тумором обогаћене, клонално амплификоване Т ћелије
Само мањина Т ћелија које инфилтрирају туморско ткиво је пријављена као специфична за туморске антигене (мање од 10%). Стога се већина интратуморских Т ћелија назива посматрачким Т ћелијама (посматрачким Т ћелијама). Најјача корелација са бројем конвенционалних Т ћелија са продуктивним ТЦР-има примећена је у субпопулацијама стромалних ћелија и леукоцита (детектовано РНК-секвенцирањем), што се може користити за процену субпопулација Т ћелија (Слика 2а). У ICR кластерима (укупна и CMS класификација), највећа клоналност имуних SEQ ТЦР-ова примећена је у ICR-високим и CMS подтиповима CMS1/имунолошка групама (Слика 2ц), са највећим уделом ICR-високих тумора. Користећи цео транскриптом (18.270 гена), шест ICR гена (IFNG, STAT1, IRF1, CCL5, GZMA и CXCL10) били су међу десет најбољих гена позитивно повезаних са клоналношћу имуних SEQ ТЦР-а (Слика 2д). Клоналност ImmunoSEQ TCR је јаче корелирала са већином ICR гена него корелације примећене коришћењем тумор-реактивних CD8+ маркера (слика 2f и 2g). Закључно, горња анализа сугерише да ICR потпис обухвата присуство тумором обогаћених, клонално амплификованих Т ћелија и може објаснити његове прогностичке импликације.
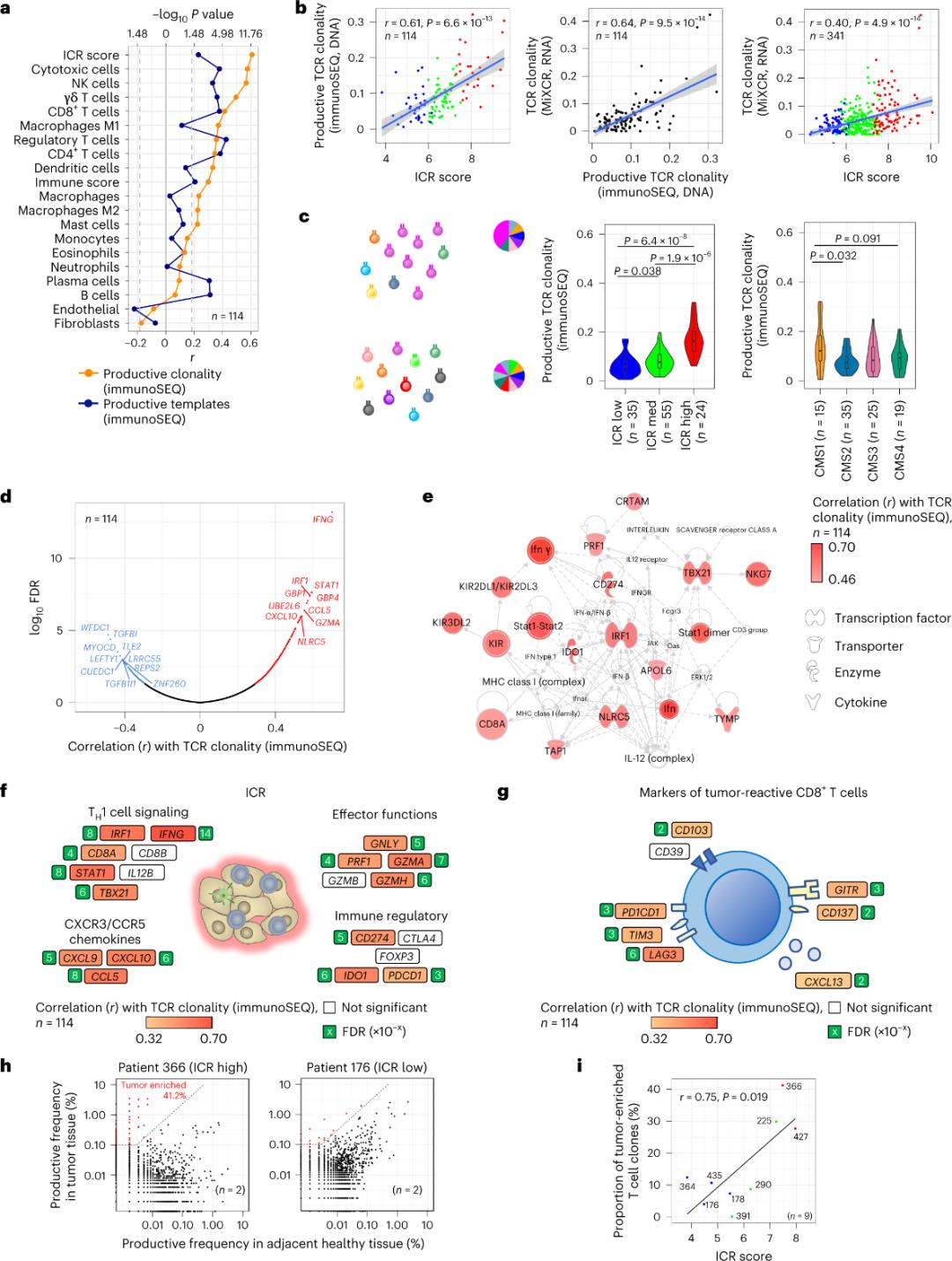
Слика 2. TCR метрике и корелација са имунолошки повезаним генима, имунолошким и молекуларним подтиповима.
Састав микробиома у здравим ткивима и ткивима рака дебелог црева
Истраживачи су извршили секвенцирање 16S рРНК користећи ДНК екстраховану из упареног туморског и здравог ткива дебелог црева од 246 пацијената (Слика 3а). Ради валидације, истраживачи су додатно анализирали податке секвенцирања гена 16S рРНК из додатних 42 узорка тумора који нису имали упарену нормалну ДНК доступну за анализу. Прво, истраживачи су упоредили релативну количину флоре између упарених тумора и здравог ткива дебелог црева. Clostridium perfringens је био значајно повећан у туморима у поређењу са здравим узорцима (Слике 3а-3д). Није било значајне разлике у алфа разноврсности (разноврсност и количина врста у једном узорку) између туморских и здравих узорака, а примећено је умерено смањење микробне разноврсности код тумора са високим ICR у односу на туморе са ниским ICR.
Да би открили клинички релевантне везе између микробних профила и клиничких исхода, истраживачи су циљали да користе податке секвенцирања гена 16S рРНК како би идентификовали карактеристике микробиома које предвиђају преживљавање. У AC-ICAM246, истраживачи су спровели OS Cox регресиони модел који је одабрао 41 карактеристику са коефицијентима који нису нула (повезаним са диференцијалним ризиком од смртности), названим MBR класификатори (слика 3ф).
У овој обучној кохорти (ICAM246), низак резултат MBR-а (MBR<0, низак MBR) био је повезан са значајно мањим ризиком од смрти (85%). Истраживачи су потврдили везу између ниског MBR-а (ризика) и продуженог OS-а у две независно валидиране кохорте (ICAM42 и TCGA-COAD). (Слика 3) Студија је показала јаку корелацију између ендогастричних коки и резултата MBR-а, који су били слични у туморском и здравом ткиву дебелог црева.
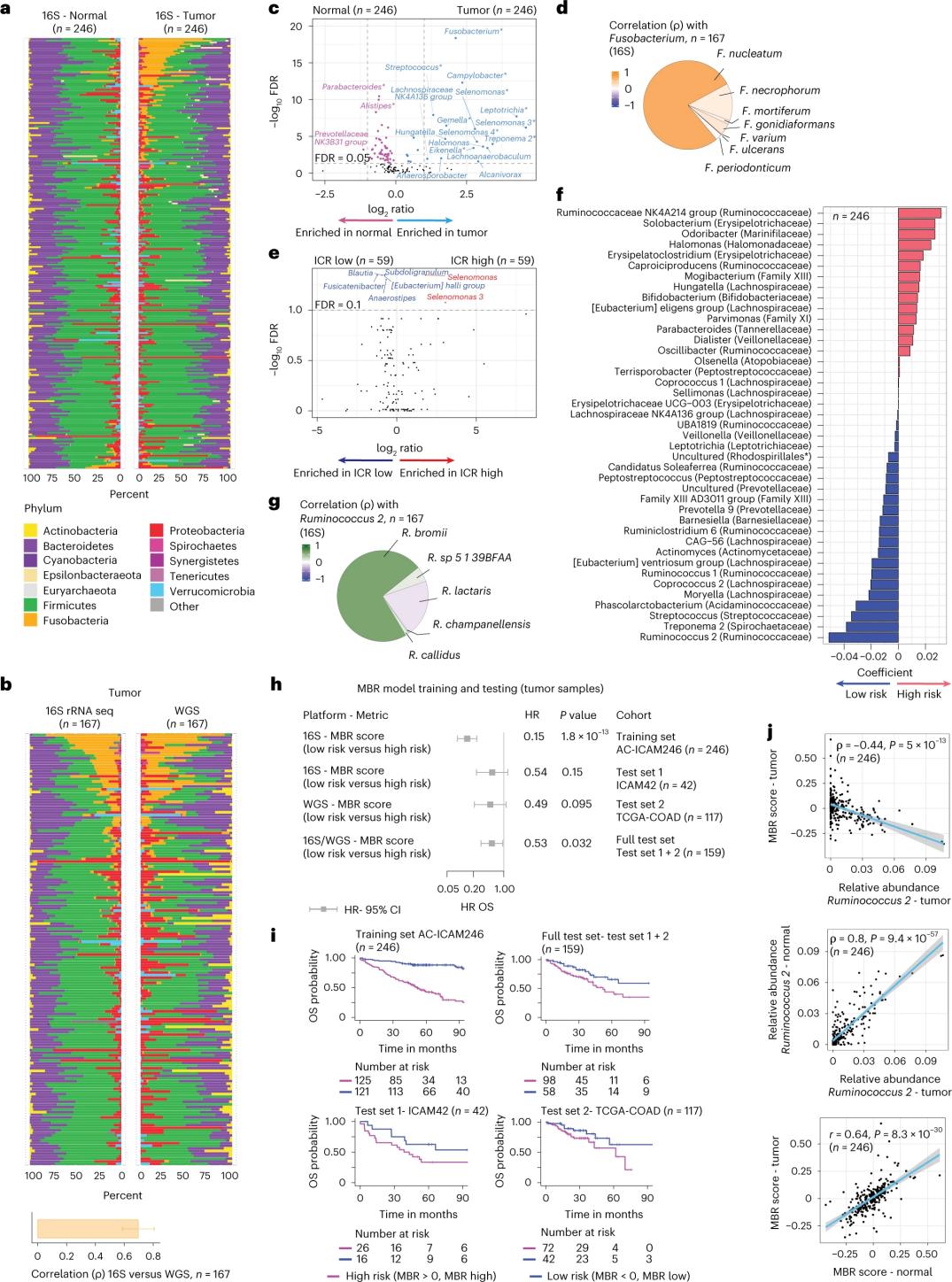
Слика 3. Микробиом у тумору и здравим ткивима и веза са ICR и преживљавањем пацијената.
Закључак
Мултимички приступ коришћен у овој студији омогућава темељну детекцију и анализу молекуларног потписа имуног одговора код колоректалног карцинома и открива интеракцију између микробиома и имуног система. Дубинско секвенцирање Т-ћелија тумора и здравих ткива открило је да прогностички ефекат ИЦР-а може бити последица његове способности да ухвати клонове Т-ћелија обогаћене тумором и могуће туморски антиген-специфичне.
Анализирајући састав туморског микробиома коришћењем секвенцирања гена 16S рРНК у AC-ICAM узорцима, тим је идентификовао микробиомски потпис (MBR скор ризика) са јаком прогностичком вредношћу. Иако је овај потпис изведен из узорака тумора, постојала је јака корелација између здравог колоректума и MBR скора ризика тумора, што сугерише да овај потпис може обухватити састав цревног микробиома пацијената. Комбиновањем ICR и MBR резултата, било је могуће идентификовати и валидирати мулти-омски студентски биомаркер који предвиђа преживљавање код пацијената са раком дебелог црева. Мулти-омски скуп података студије пружа ресурс за боље разумевање биологије рака дебелог црева и помоћ у откривању персонализованих терапијских приступа.
Време објаве: 15. јун 2023.
 中文网站
中文网站